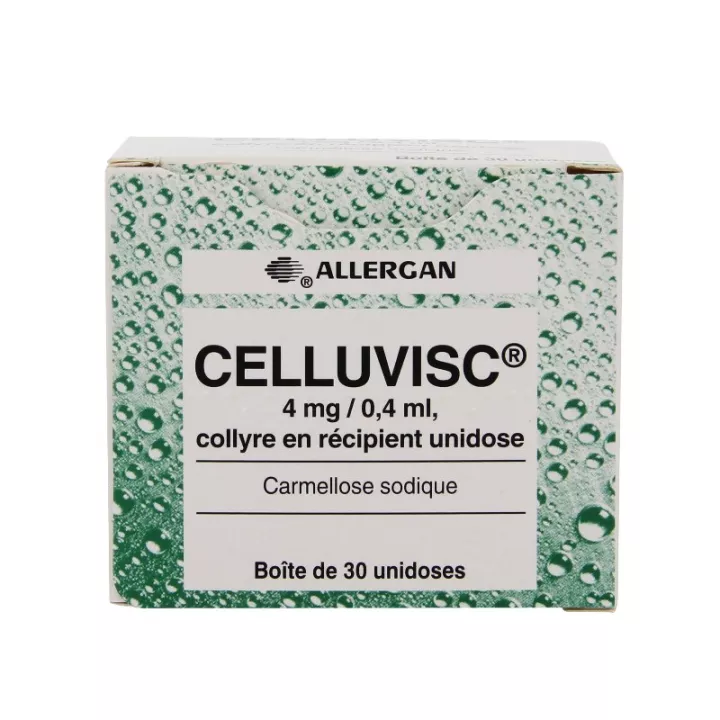
¿Cuáles son las indicaciones del colirio Celluvisc en monodosis?
Este medicamento de venta libre está indicado para tratar los signos de irritación causados por la sequedad ocular (cuando el lagrimeo es insuficiente).
Este colirio es transparente e incoloro. Las gotas para los ojos Celluvisc 4mg / 0.4ml no son reutilizables.
¿Cómo utilizar correctamente estas dosis contra la sequedad ocular?
Siga siempre la posología indicada por su médico. En caso de duda, consulte a un profesional de la salud. La dosis habitual es de 1 gota en el ojo de 2 a 4 veces al día y hasta 8 veces al día si persiste el ojo seco.
Comente las recomendaciones de uso y la dosificación de Celluvisc Eye Drops Eye Dryness en dosis únicas con nuestro socio Avis verificado después de su compra .
- Despegue una sola dosis del blíster.
- Sostenga la dosis única verticalmente, la tapa debe colocarse hacia arriba. Para abrir la monodosis, girar completamente la parte plana para romper el precinto.
- Tire suavemente del párpado inferior hacia abajo mientras mira hacia arriba. Voltee la dosis única y apriétela suavemente para dispensar 1 gota en el(los) ojo(s) a tratar. Parpadea varias veces.
¿Cuál es la composición de este colirio Celluvisc?
El principio activo es: Carmelosa sódica .......... 4,00 mg Para envase monodosis.
Los demás componentes son: cloruro de sodio, lactato de sodio, cloruro de potasio, cloruro de calcio, agua purificada.
¿Cuáles son las precauciones de uso ?
Una sola dosis es suficiente para tratar ambos ojos, no es reutilizable. Utilizar una nueva monodosis con cada nueva aplicación del día.
Asegúrese de que sus manos estén limpias antes de usar este producto. La punta de dosificación no debe entrar en contacto con el ojo ni con ninguna otra superficie. No use la dosis única si la tapa parece rota antes de usar.
Presentación - Empaque
Celluvisc Collyre Sécheresse ocular está disponible en nuestra farmacia online en cajas que contienen 30 monodosis.