Antiestetiche e talvolta dolorose, le verruche e i calli possono diventare rapidamente un fastidio nella vita quotidiana. Soin-et-Nature offre trattamenti farmaceutici e naturali che combinano un'efficacia comprovata, una tolleranza ottimale e la facilità di utilizzo a casa. Che si tratti di creme cheratolitiche, soluzioni crioterapiche o dispositivi di protezione, ogni trattamento è selezionato per agire rapidamente, alleviare il disagio e aiutare la pelle a ritrovare la sua morbidezza e integrità, in tutta sicurezza.
Maggiori dettagli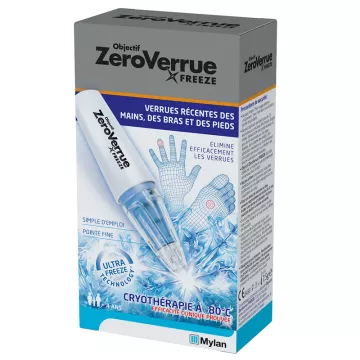
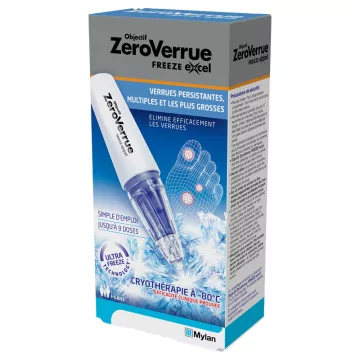
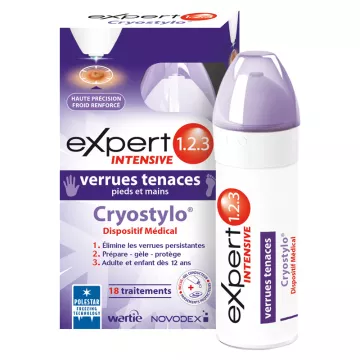

Le verruche e i calli sono molto più di un inconveniente estetico: possono diventare rapidamente dolorosi, fastidiosi e persino limitare i movimenti. Le verruche sono causate da un virus (il papillomavirus umano, o HPV), mentre i calli derivano dallo sfregamento ripetuto o dalla pressione eccessiva su una zona del piede.
Fin dall'antichità sono state sviluppate diverse soluzioni per combattere questi problemi. Dalle piante medicinali ai trattamenti moderni, l'obiettivo rimane lo stesso: eliminare la verruca o il corno rispettando la pelle. Oggi, grazie alle innovazioni farmaceutiche, è possibile accedere a trattamenti rapidi, sicuri e adatti a tutti, comodamente da casa.
I nostri valori? Accessibilità, efficacia e rispetto della pelle. Crediamo che tutti meritino il comfort di camminare senza dolore e la sicurezza di mostrare mani e piedi senza imbarazzo. Per questo offriamo un'ampia gamma di soluzioni facili da usare a casa.
La lotta contro verruche e calli si basa su metodi adeguati alla situazione. Ecco le principali famiglie di trattamenti disponibili nella nostra categoria:
Ogni metodo ha i suoi vantaggi, a seconda della natura, dell'età e della posizione della verruca o del corno. Sta a voi scegliere quello più adatto alle vostre esigenze!
Spesso si dice cheun grammo di prevenzione vale un chilo di trattamento. Ecco alcuni semplici accorgimenti da adottare:
Seguendo questi semplici consigli, avrete tutte le possibilità di evitare recidive e nuovi focolai.
Quando si tratta di verruche e calli, non lasciateli in giro. Più una verruca è vecchia, più è ancorata in profondità nel tessuto, rendendo il trattamento più lungo e doloroso.
Il farmacista consiglia di
Con l'aiuto del vostro farmacista, potrete massimizzare le possibilità di un trattamento di successo e senza complicazioni.
Voleteottimizzare il vostro trattamentoin modo naturale? Ecco alcuni consigli ispirati alla natura:
Questi approcci dolci non sostituiscono i trattamenti convenzionali, ma li integrano armoniosamente per un'azione più completa e duratura.
La nostra farmacia online offre una gamma completa di prodotti dermatologici per diverse condizioni della pelle, suddivisi in varie categorie per una cura ottimale: