A cosa serve Mycoster 1% Soluzione 30 ml?
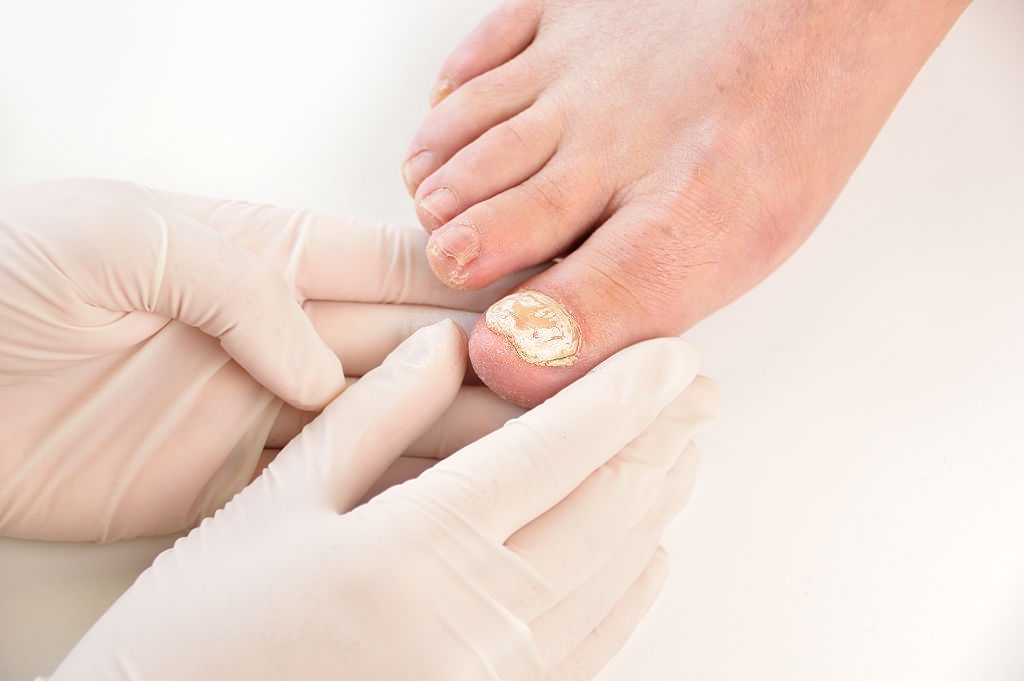
Mycoster 1% Soluzione 30 ml è un medicinale indicato per il trattamento delle infezioni fungine della pelle o delle unghie , infettate o meno da batteri, e della dermatite seborroica del viso da lieve a moderata.
I funghi che causano infezioni nell'uomo sono ben noti. I principali responsabili sono i dermatofiti che colpiscono la pelle e alcuni lieviti, come la Candida per le micosi vaginali e la Pityriasis versicolor che causa macchie pigmentate. Ma anche altri funghi meno conosciuti possono dilagare.
Che cos'è una micosi? Molti funghi prosperano sulla pelle e sulle mucose. Normalmente innocui, questi ospiti sfruttano le debolezze del nostro sistema immunitario per diventare talvolta molto invasivi.
A seconda della loro localizzazione, le micosi possono essere superficiali, cutanee, sottocutanee o profonde (generalizzate);
modalità di trasmissione: l'agente causale può essere endogeno (naturalmente presente nell'organismo) o esogeno (trasmesso per via respiratoria, cutanea o transcutanea);
in base alla gravità: la maggior parte delle micosi non è grave (micosi vaginali, micosi delle unghie, ecc.), ma le infezioni fungine che si verificano in soggetti indeboliti, in particolare in ospedale, possono essere fatali.
Trattare le infezioni fungine della pelle e delle unghie con Mycoster 1% Soluzione
I funghi della pelle e delle unghie possono essere fastidiosi e imbarazzanti. Mycoster 1% Soluzione 30ml è appositamente formulato per trattare efficacemente queste micosi, lasciandovi una pelle e delle unghie sane.
Perché scegliere Mycoster 1% Soluzione 30ml?
1. Trattamento completo
Questa soluzione è stata studiata per trattare le infezioni fungine della pelle e delle unghie. Offre un approccio completo per eliminare i funghi responsabili di queste condizioni.
2. Azione antimicotica
Mycoster 1% Solution contiene un potente agente antimicotico che agisce direttamente sui funghi. Li elimina efficacemente per un rapido sollievo.
3. Applicazione pratica
L'applicazione della soluzione è semplice e comoda. Utilizzate l'applicatore per stendere la soluzione sull'area interessata per un'azione mirata.
4. Formato conveniente
Il flacone da 30 ml di Mycoster 1% Solution è facile da trasportare, in modo da poterlo utilizzare ovunque.
5. Marchio affidabile
Mycoster è un marchio affidabile nell'industria farmaceutica, riconosciuto per il suo impegno nella qualità e nell'efficacia dei suoi prodotti.
Come si usa Mycoster 1% Soluzione 30 ml?
Il dosaggio di Mycoster 1% dipende dal tipo di patologia da trattare. Nel caso delle micosi cutanee, saranno necessarie 2 applicazioni giornaliere per circa 21 giorni, mentre le micosi ungueali saranno trattate applicando la soluzione per diversi mesi.
Infine, la dermatite seborroica sarà trattata inizialmente con 2 applicazioni al giorno per 2-4 settimane, seguite da 1 applicazione al giorno per 28 giorni. SEGUIRE LA PRESCRIZIONE DEL MEDICO. Metodo e via di somministrazione Pelle. Durata del trattamento Seguire le indicazioni del medico.
Esprimi la tua opinione sui consigli d'uso e sul dosaggio di Mycoster 1% Soluzione 30ml con il nostro partner Opinioni verificate dopo l'acquisto.
FAQ su Mycoster 1% Soluzione 30ml
1. Come si usa Mycoster 1% Soluzione 30ml?
Applicare la soluzione sulla zona interessata come indicato dal medico. Utilizzare l'applicatore per un'applicazione precisa.
2. Quanto tempo ci vuole per vedere i risultati?
I risultati possono variare a seconda della gravità dell'infezione. In generale, si dovrebbe iniziare a notare un sollievo dai sintomi entro poche settimane.
3. Ci sono effetti collaterali di cui preoccuparsi?
La maggior parte degli utilizzatori di Mycoster 1% Soluzione non manifesta effetti collaterali gravi. Tuttavia, se si verifica una reazione cutanea grave, interrompere l'uso e consultare un medico.
4. Posso usare questa soluzione su altre parti del corpo?
Mycoster 1% Soluzione è specificamente indicato per le infezioni fungine della pelle e delle unghie. Si raccomanda di consultare un medico per altre condizioni della pelle.
5. Dove posso acquistare Mycoster 1% Soluzione 30ml?
Potete acquistare Mycoster 1% Soluzione 30ml nella vostra farmacia locale o online con fiducia. È disponibile per offrirvi un trattamento efficace per i funghi della pelle e delle unghie. Non aspettate che il disagio persista, ordinate ora e recuperate pelle e unghie sane con Mycoster 1% Soluzione 30ml.
Mycoster 1% Soluzione 30ml è il vostro alleato per eliminare le infezioni fungine della pelle e delle unghie. Non lasciate che queste condizioni vi disturbino, scegliete la soluzione di fiducia per una pelle e unghie sane. Ordinate oggi stesso e prendetevi cura della vostra pelle e delle vostre unghie con Mycoster 1% Soluzione 30ml.
Cosa contiene questa soluzione contro le infezioni fungine?
Ciclopirox olamina ............ 1.000 g per 100 ml di soluzione.
Gli altri ingredienti sono: Macrogol 400, isopropanolo, acqua depurata.
Quali sono gli effetti collaterali e le controindicazioni?
Questo farmaco è solo per uso esterno.
Se ritiene che l'effetto di MYCOSTER 1%, soluzione per applicazione cutanea sia troppo forte o troppo debole, consulti il medico o il farmacista. Solo per uso esterno.
Presentazione - Confezione
Mycoster 1% soluzione si presenta in un tubo da 30 ml.